- · 《中国组织工程研究》栏[05/29]
- · 《中国组织工程研究》数[05/29]
- · 《中国组织工程研究》收[05/29]
- · 《中国组织工程研究》投[05/29]
- · 《中国组织工程研究》征[05/29]
- · 《中国组织工程研究》刊[05/29]
《Cell》MIT:基于水凝胶的组织转化技术的基本原(2)
作者:网站采编关键词:
摘要:图 3 组织凝胶特性的优化。 机械韧性 这是一种材料在高应力下承受断裂的能力(强度的衡量标准),即使变形到高应变(可变形性的衡量标准),它通常
图 3 组织凝胶特性的优化。
机械韧性
这是一种材料在高应力下承受断裂的能力(强度的衡量标准),即使变形到高应变(可变形性的衡量标准),它通常被量化为材料应力-应变曲线下方的面积(图 3D)。 对于大多数组织转化应用,需要坚固但不可变形(即中等韧性)的刚性组织凝胶(图 3E)。然而,保持高强度同时具有高度可拉伸性或可压缩性的更坚韧的组织凝胶显着降低脆性、更耐损坏且不易撕裂(图 3F)。
将基于水凝胶的方法扩展到体积样品的挑战
水凝胶网的一个重要作用是在脂质去除步骤(脱脂)期间将生物分子固定在其生理位置。 内源性脂质层充当物理和光学屏障,分别阻止分子探针和光子的细胞内递送(图 4A)。因此,不同程度的脱脂已被用于组织清除和转化方法,以增加生物组织的分子渗透性和光学透明度。特别是基于合成凝胶的方法,允许使用强洗涤剂完全脱脂,因为即使在完全去除脂质双层后,水凝胶网也可以防止生物分子及其空间组织的损失(图 4A)。
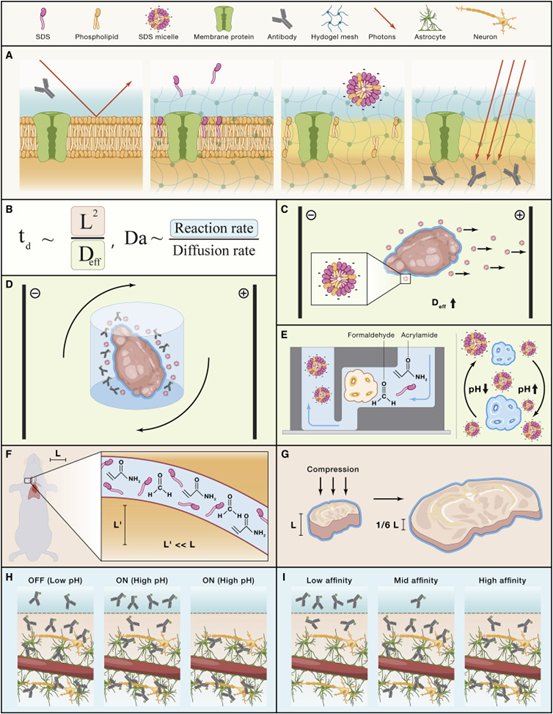
图 4 组织清除和分子递送的基本原理。
组织转化技术的应用
空间转录组
分析各种细胞类型的空间组织及其基因表达对于理解复杂生物系统中的结构-功能关系至关重要。原位转录组学技术的最新进展使基因表达的空间映射变得越来越高分辨率和多路复用。例如,smFISH 可以在其天然组织环境中以单细胞分辨率绘制单个 RNA 分子(图 5A 和 5B)。smFISH 中的空间、光谱和顺序条码方法已经能够在单个细胞中绘制许多 RNA 种类(图 5C 和 5D)。

图5 基于杂交的空间转录组分析概述
另一种原位转录组学方法直接在感兴趣的细胞/组织内对 mRNA 进行测序。例如,原位测序(图 6A)和荧光原位 RNA 测序(FISSEQ)(图 6B)在生物样品中生成互补 DNA (cDNA) 扩增子,并通过反复杂交和成像荧光探针对扩增子进行测序。同样,水凝胶辅助的原位测序方法,空间分辨转录扩增子读出映射(STARmap),直接在厚组织内生成 cDNA 纳米球(扩增子)(图 6C 和 6D)。

图6 基于测序的空间转录组分析概述
蛋白质组
蛋白质组成像技术的最新进展克服了这些挑战,使研究人员能够从组织切片中提取前所未有的蛋白质组学细节。例如,Angelo 等人,2014 年通过使用多路复用离子束成像 (MIBI) 和基于质谱的检测在 4 微米厚的组织切片中同时对 10 个金属标记抗体(可扩展到 100 个目标)进行成像,研究了肿瘤组织中的细胞异质性(图7A和7B)。这些金属标记方法只需要一轮抗体孵育,而基于质谱的方法没有自发荧光,这使得它们成为绘制薄组织切片中二维蛋白质分布图的有吸引力的选择。类似地,包括 CODEX(Goltsev 等人,2018 年)、可扩散探针(Guo 等人,2019 年)和 Immuno-SABER(Saka 等人,2019 年)在内的条形码方法能够使用寡核苷酸文库对组织切片进行单轮标记-偶联抗体,用独特的核苷酸序列编码每个靶标(图 7C 和 7D)。然后使用荧光核苷酸杂交的重复循环对标记的抗体进行成像,从而使同一薄组织切片内的数十个目标能够可视化。对于 3D 蛋白质组学组织分析,阵列断层扫描已被广泛使用(Micheva 和 Smith,2007)。阵列断层扫描将组织嵌入塑料树脂中,然后进行连续切片、多轮染色和切片阵列成像(图 7E)。

图 7 空间蛋白质组和连接组分析概述。
【总结】
基于水凝胶的组织转化技术的优势在于,研究人员可以轻松修改理化特性,以从完整组织中保存和提取丰富的分子、解剖和功能信息。在这篇综述中,探讨了基于水凝胶的组织转化方法的现状,并概述了它们的基本原理,以帮助研究人员选择、优化和战略性地结合研究技术。此外,该团队讨论了扩大 3D 原位分子表型的困难,并介绍了直接应对挑战的新兴技术。
文章来源:《中国组织工程研究》 网址: http://www.zgzzgcyj.cn/zonghexinwen/2021/0811/1818.html